こんにちは。愛知県豊橋市で脳梗塞・脳出血専門の自費リハビリ施設である脳梗塞リハビリスタジオActiveの代表、戀田祐司です!
今回は初めてご来店される方から、ほぼ100%質問されるあることについて解説していきます。
「発症から1年以上経った。もうリハビリに意味はないのか」
その問いを抱えたまま、通院を続けている方や、自宅でひとり動かし続けている方が少なくありません。担当の医師やセラピストから「回復はプラトーに達している」と言われた経験がある方もいるかもしれません。
結論から述べます。発症から1年以上が経過していても、神経学的な変化が起きる可能性は残っています。
ただし、それは「誰にでも」「いつでも」起きるわけではなく、残存する神経基盤と介入の質・量が条件として関わってきます。
この記事では、自発的回復と学習による回復を区別した上で、慢性期に変化が生じうる神経メカニズムと、変化しにくい状態の特徴、そして慢性期リハビリのエビデンスを整理します。
感情的な励ましではなく、現時点で分かっていることと分かっていないことを、できるかぎり正確にお伝えします。
自発的回復と学習による回復は別物である
「発症から6ヶ月で回復の窓が閉まる」「1年を過ぎると変化しない」——こうした言葉が一人歩きしている背景には、自発的回復と学習による回復の混同があります。この2つは、起きているプロセスが根本的に異なります。
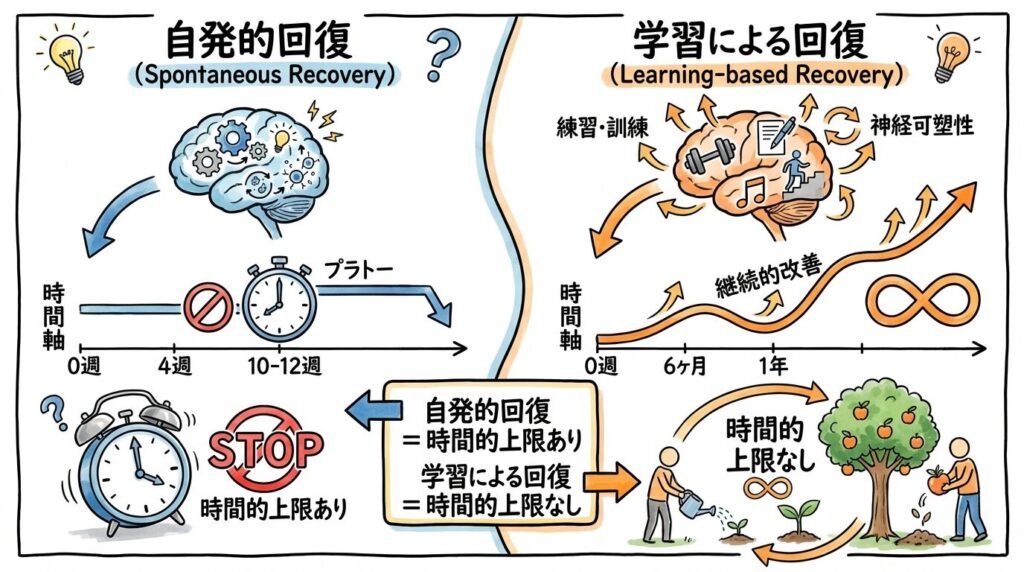
自発的回復:神経学的なプラトーは発症後10〜12週前後
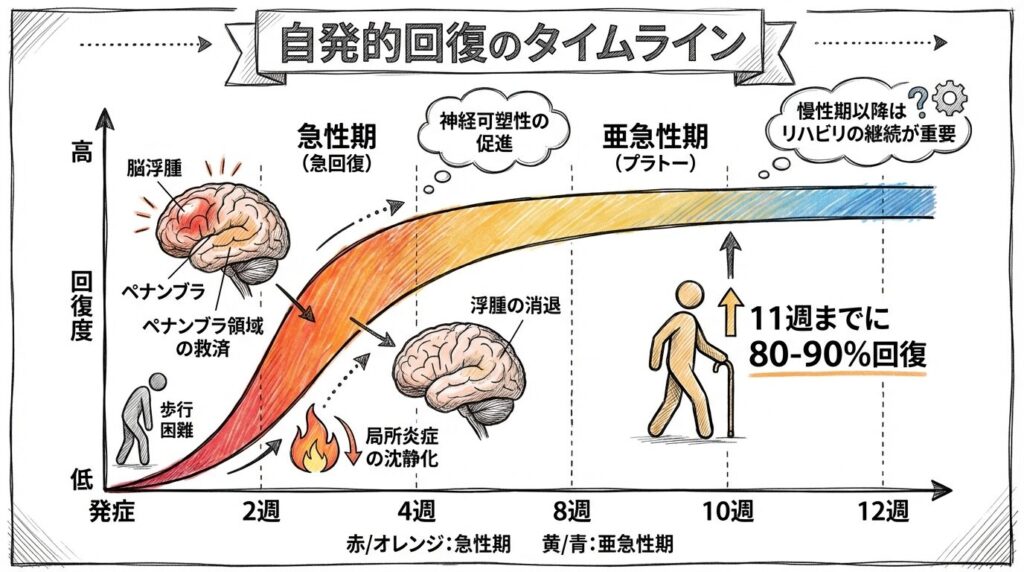
自発的回復(spontaneous neurological recovery)とは、脳梗塞や脳出血後に、浮腫の消退・局所炎症の沈静化・ペナンブラ(梗塞周辺の生存組織)の機能回復などによって、特別な介入がなくても機能が改善に向かうプロセスです。
この自発的回復は、発症から数週間で最も著明であり、発症後10〜12週ごろには大部分が終結するとされています。Jorgensen ら(1995)は、脳卒中後の歩行機能の自発的回復の80〜90%が発症後11週までに生じることを示しており、この期間は特に注目されてきました。
重要なのは、この「プラトー」が指しているのはあくまで自発的回復の終息であり、脳の可塑性が止まることを意味するわけではないという点です。
学習による回復:時間的な上限は設けられていない
学習による回復(learning-based recovery)は、反復的な練習・課題に対する経験・適切な負荷によって、シナプス接続が強化・再編されることで機能が変化するプロセスです。これは運動学習と同じ原理に立っており、発症から何年が経過していても、条件が整えば起きる可能性があります。
Nudo ら(1996)のサルを用いた研究では、脳梗塞後に集中的な課題指向型トレーニングを行った群で、梗塞周辺の一次運動野に代替的な運動表現(cortical map reorganization)が生じたことが示されています。この研究は動物を対象としたものであり、ヒトへの直接的な適用には慎重であるべきですが、学習依存的な可塑性が慢性期にも残存しうることを示す重要な知見として位置づけられています。
「回復はもう終わった」という認識は、自発的回復の終息と脳の可塑性の終息を同一視した誤解から生まれやすいものです。
慢性期でも変化が起きうる神経のメカニズム
慢性期に変化が生じる根拠として、現在の神経科学研究が示しているのは主に以下の3つのプロセスです。
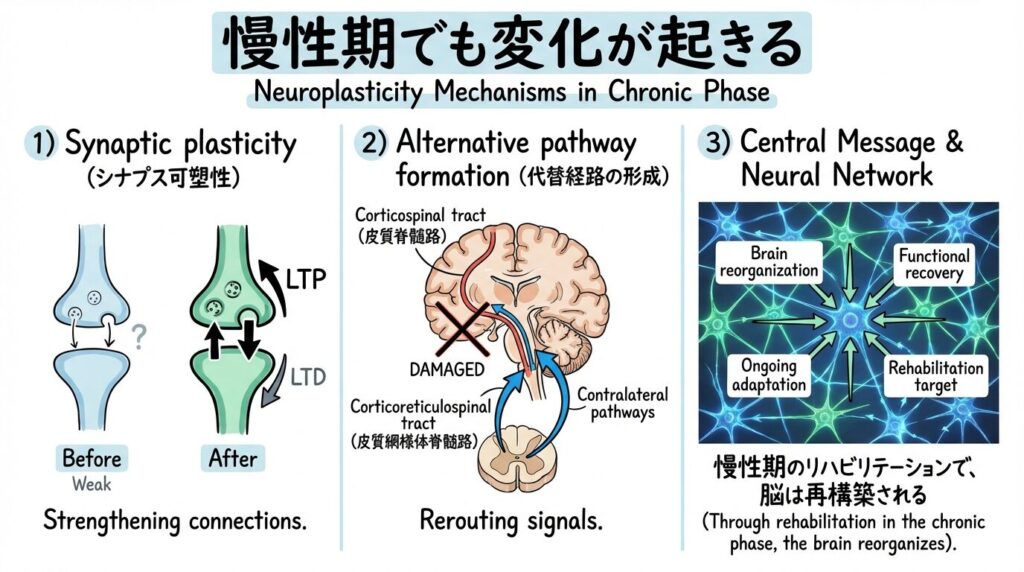
シナプス可塑性
繰り返しの神経活動によって、シナプスの結合効率が変化する現象を指します。長期増強(LTP: Long-Term Potentiation)と長期抑圧(LTD: Long-Term Depression)がその代表であり、いずれも適切な入力が繰り返されることで生じます。動物実験では、脳梗塞後の慢性期においてもLTPが誘導できることが示されており、ヒトの慢性期においても経頭蓋磁気刺激(TMS)を用いた研究でシナプス可塑性の残存が確認されています(Bütefisch et al., 2000)。
代替経路の形成
皮質脊髄路(corticospinal tract)が損傷を受けた場合でも、皮質網様体脊髄路(corticoreticulospinal tract)や対側半球からの経路が、運動機能の一部を代償的に担う可能性が示されています。この代替経路は、完全に新しい回路が「生えてくる」のではなく、もともと存在していた副次的な経路が相対的に強化されるという形で機能を担います。代償(compensation)と回復(recovery)の中間に位置するプロセスであり、臨床的に「動きが変わった」と感じられる変化の一部はこの機序によるものと考えられます。
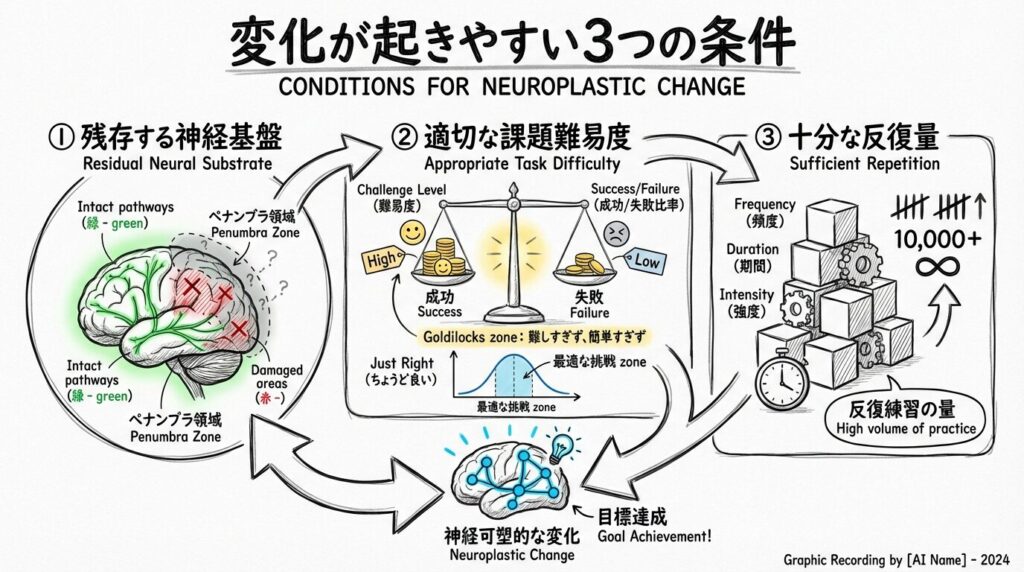
変化が起きやすい3つの条件
神経可塑性が生じやすくなる条件として、研究から示されているのは以下の通りです。
第一に、残存する神経基盤があることです。完全に梗塞に巻き込まれた経路では可塑的変化の余地は極めて乏しく、ペナンブラや損傷を免れた隣接経路が残っているほど変化が生じやすいとされています。
第二に、課題難易度が適切であることです。難しすぎず、かつ単純すぎない——あるいは成功と失敗が繰り返される負荷設定が、神経可塑性を引き出す上で重要とされています(Kleim & Jones, 2008)。
第三に、十分な反復量があることです。Kleim & Jones(2008)は、神経可塑性を生じさせるためには相当数の反復が必要であることを強調しており、数回の練習では不十分であることを示しています。Lohse ら(2014)のメタ解析では、上肢機能改善のために必要な練習量が現在の標準的なリハビリの提供量を大きく上回る可能性が示されており、量的な課題は慢性期を問わず共通しています。
変化しにくい状態とはどんなものか
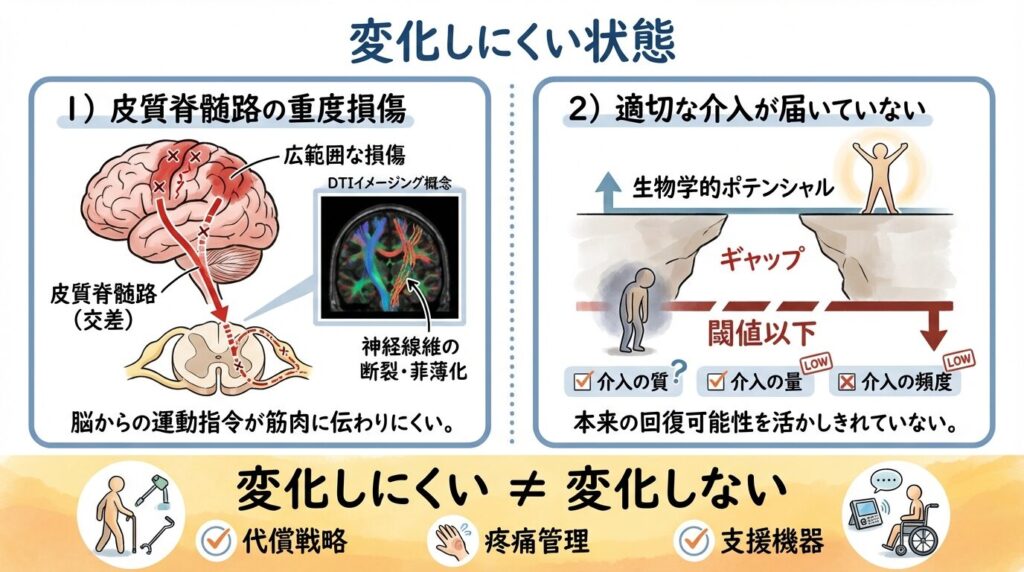
慢性期に変化が起きる可能性を示す一方で、変化が生じにくい状態についても誠実に整理する必要があります。「変化しにくい」と「変化しない」は同義ではありませんが、その区別を曖昧にすることも適切ではありません。
皮質脊髄路の重度損傷がある場合
随意運動の主要な経路である皮質脊髄路が広範かつ高度に損傷されている場合、その経路を通じた随意的な運動回復の余地は限られます。拡散テンソル画像(DTI)を用いた研究では、内包後脚における皮質脊髄路の線維残存率が上肢機能の回復予後と相関することが示されています(Stinear et al., 2007)。ただし、これは「重症だから何も変わらない」ではなく、「どの経路でどの機能を回復・代償の目標とするか」を吟味する必要があるということです。
適切な介入が届いていない場合
生物学的な可塑性が残存していても、それを引き出す質と量を持った介入が提供されていなければ変化は起きません。「リハビリをやっているが変わらない」という状況の中に、介入の種類・負荷・量・頻度が可塑性を誘導する水準に達していないケースが含まれている可能性があります。これは当事者の問題ではなく、介入設計の問題です。
「変化しにくい」は「変化しない」を意味しない
重要なのは、「変化しにくい」状態であっても、代償戦略の最適化・疼痛管理・スプリント装具による機能補助・心理的負担の軽減など、生活の質に関わる目標は十分に存在するという点です。回復の余地が小さい場合でも、生活機能の向上を目指したリハビリに意味がないということにはなりません。
慢性期のリハビリに変化が起きることを示す研究
ここでは、発症後6ヶ月以降の慢性期当事者を対象とした介入研究のうち、比較的エビデンスの蓄積がある3つの領域を紹介します。
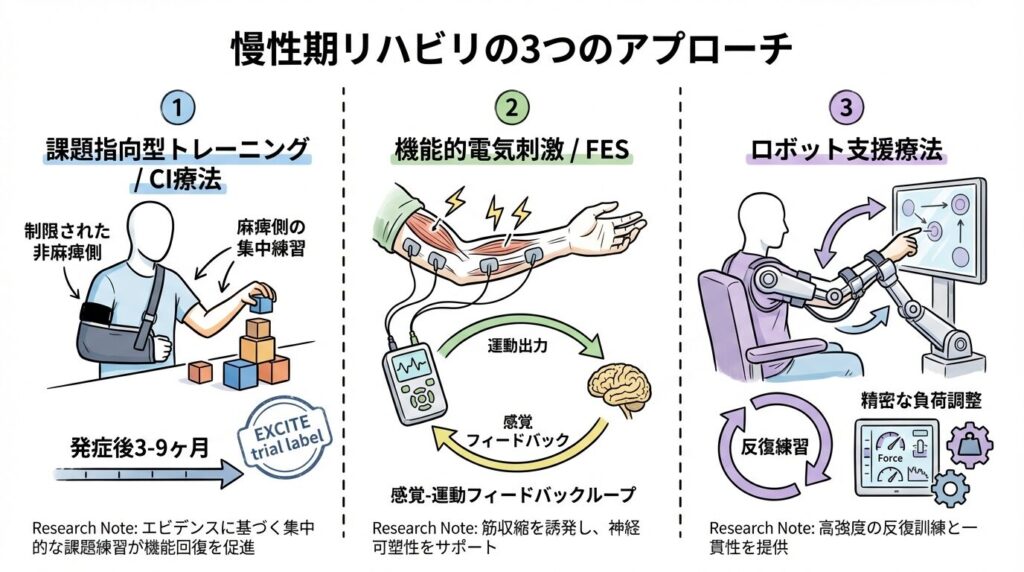
課題指向型トレーニング(Task-oriented training)
Wolf ら(2006)が実施したEXCITE試験は、発症後3〜9ヶ月の慢性期上肢麻痺患者を対象に、constraint-induced movement therapy(CI療法)の効果を検証したRCTです。CI療法群では非麻痺側上肢の使用を制限しながら麻痺側上肢の集中的な課題練習を行い、対照群と比較して上肢機能の有意な改善が12ヶ月後にも維持されることが示されました。この結果は、発症から時間が経過した慢性期においても、適切な強度・量の介入によって上肢機能に変化が生じうることを示しています。
機能的電気刺激(FES)
Peckham & Knutson(2005)のレビューおよびその後の複数のRCTにおいて、FESが慢性期上肢麻痺の機能改善に関与する可能性が示されています。FESは筋収縮を電気刺激によって誘発しつつ、感覚入力と運動出力のフィードバックループを形成することで、感覚運動皮質の再組織化を促す可能性があるとされています。ただし、効果の大きさと持続性については研究間のばらつきがあり、現時点ではすべての慢性期患者に一律に効果があるとは言えません。
ロボット支援療法
Mehrholz ら(2015)のコクランレビューでは、上肢麻痺に対するロボット支援療法が、通常のリハビリと比較して上肢機能改善に有意な効果をもたらす可能性が示されています。ロボット支援療法の特徴は、量の確保(反復回数の担保)と負荷の精密な調整が可能な点であり、慢性期においても十分な反復量を確保するための手段として位置づけられます。こちらも効果の大きさは患者特性や介入プロトコルによって異なり、どの患者に適しているかの個別評価が必要です。
発症から時間が経過している方こそ、まず評価から
「慢性期だから」「もうプラトーだから」という理由でリハビリの選択肢を狭めてしまうことが、変化の可能性そのものを閉じてしまうことがあります。
一方で、「慢性期でも変化する可能性がある」という情報だけを持って、闇雲に量だけを増やすことも適切ではありません。どの機能を目標にするか、残存する神経基盤はどの程度か、現在の介入が可塑性を引き出す水準に達しているかを、個別に評価した上で介入を設計する必要があります。
脳梗塞リハビリスタジオActiveでは、発症から時間が経過した方に対しても、電気刺激(FES含む)・振動刺激・課題指向型トレーニング・トレッドミルトレーニングをセラピストとのマンツーマンで組み合わせ、まず現状の評価から行っています。
今の状態を丁寧に評価した上で、何を優先すべきかを一緒に整理します。リハビリにお悩みの方は、ぜひ一度ご相談ください。
まとめ
発症から1年以上が経過していても、神経学的な変化の可能性が完全に消えるわけではありません。ただし、それは自発的回復の終息と混同されやすく、「プラトー=もう変わらない」という理解は正確ではありません。
学習による回復は、残存する神経基盤・適切な課題難易度・十分な反復量という条件のもとで慢性期にも起きうるものです。変化しにくい状態が存在することも事実ですが、「変化しにくい」は「変化しない」を意味せず、代償と回復のどちらを目標とするかの吟味が常に必要です。
慢性期の当事者と家族に伝えたいのは、希望と根拠はセットでなければ意味がないということです。感情的な励ましではなく、評価に基づいた見立てと、それに沿った介入こそが、変化の可能性を引き出す入口になります。
参考文献
Bütefisch, C. M., Davis, B. C., Wise, S. P., Sawaki, L., Kopylev, L., Classen, J., & Cohen, L. G. (2000). Mechanisms of use-dependent plasticity in the human motor cortex. Proceedings of the National Academy of Sciences, 97(7), 3661–3665. https://doi.org/10.1073/pnas.050350297
Jorgensen, H. S., Nakayama, H., Raaschou, H. O., Vive-Larsen, J., Støier, M., & Olsen, T. S. (1995). Outcome and time course of recovery in stroke. Part II: Time course of recovery. The Copenhagen Stroke Study. Archives of Physical Medicine and Rehabilitation, 76(5), 406–412. https://doi.org/10.1016/S0003-9993(95)80568-0
Kleim, J. A., & Jones, T. A. (2008). Principles of experience-dependent neural plasticity: Implications for rehabilitation after brain damage. Journal of Speech, Language, and Hearing Research, 51(1), S225–S239. https://doi.org/10.1044/1092-4388(2008/018)
Lohse, K. R., Lang, C. E., & Boyd, L. A. (2014). Is more better? Using metadata to explore dose–response relationships in stroke rehabilitation. Stroke, 45(7), 2053–2058. https://doi.org/10.1161/STROKEAHA.114.004695
Mehrholz, J., Pohl, M., Platz, T., Kugler, J., & Elsner, B. (2015). Electromechanical and robot-assisted arm training for improving activities of daily living, arm function, and arm muscle strength after stroke. Cochrane Database of Systematic Reviews, (11), CD006876. https://doi.org/10.1002/14651858.CD006876.pub4
Nudo, R. J., Wise, B. M., SiFuentes, F., & Milliken, G. W. (1996). Neural substrates for the effects of rehabilitative training on motor recovery after ischemic infarct. Science, 272(5269), 1791–1794. https://doi.org/10.1126/science.272.5269.1791
Peckham, P. H., & Knutson, J. S. (2005). Functional electrical stimulation for neuromuscular applications. Annual Review of Biomedical Engineering, 7, 327–360. https://doi.org/10.1146/annurev.bioeng.6.040803.140103
Stinear, C. M., Barber, P. A., Smale, P. R., Coxon, J. P., Fleming, M. K., & Byblow, W. D. (2007). Functional potential in chronic stroke patients depends on corticospinal tract integrity. Brain, 130(1), 170–180. https://doi.org/10.1093/brain/awl333
Wolf, S. L., Winstein, C. J., Miller, J. P., Taub, E., Uswatte, G., Morris, D., Giuliani, C., Light, K. E., Nichols-Larsen, D., & EXCITE Investigators. (2006). Effect of constraint-induced movement therapy on upper extremity function 3 to 9 months after stroke: The EXCITE randomized clinical trial. JAMA, 296(17), 2095–2104. https://doi.org/10.1001/jama.296.17.2095